Marktübersicht für Electronic Trial Master File (eTMF)-Systeme
pLaut MRFR-Analyse wird die Größe des Marktes für Electronic Trial Master File Systeme im Jahr 2024 auf 1,02 Milliarden US-Dollar geschätzt. Der Markt für Electronic Trial Master File Systeme wird voraussichtlich von 1,16 Milliarden US-Dollar im Jahr 2025 auf 3,81 Milliarden US-Dollar bis 2034 wachsen, bei einer CAGR (Wachstumsrate) von voraussichtlich etwa 14,12 % während des Prognosezeitraums (2025–2034). Die Einhaltung gesetzlicher Vorschriften, Effizienz und Kosteneinsparungen sowie die zunehmende Nutzung elektronischer Aufzeichnungen sind die wichtigsten Markttreiber, die das Marktwachstum fördern.
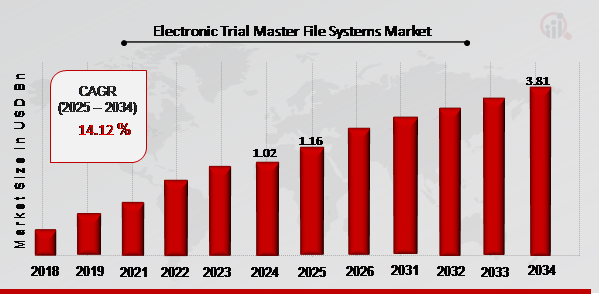
Quelle: Sekundärforschung, Primärforschung, MRFR-Datenbank und Analystenbewertung
Markttrends für Electronic Trial Master File (eTMF)-Systeme
h3
Zunehmende Nutzung elektronischer Aufzeichnungen fördert Marktwachstum pDie Pharma- und Biotech-Branche ist stark reguliert, und eTMF-Systeme bieten Unternehmen eine Möglichkeit, ihre Dokumentation klinischer Studien in Übereinstimmung mit Vorschriften wie 21 CFR Part 11 zu verwalten. Dies war ein bedeutender Wachstumsfaktor für eTMF-Systeme, da Unternehmen das Risiko von Strafen wegen Nichteinhaltung vermeiden und ihre Prozesse zur behördlichen Berichterstattung rationalisieren möchten.
eTMF-Systeme können die Effizienz klinischer Studien verbessern, indem sie den Zeit- und Arbeitsaufwand für die Verwaltung der Studiendokumentation reduzieren. Dies kann zu Kosteneinsparungen für Unternehmen führen, da sie weniger Ressourcen zur Verwaltung ihrer Studien benötigen. Eine Studie des Tufts Center for the Study of Drug Development hat beispielsweise ergeben, dass eTMF-Systeme den Zeitaufwand für die Fertigstellung der Dokumentation klinischer Studien um bis zu 10 % reduzieren können.
eTMF-Systeme ermöglichen eine bessere Zusammenarbeit und einen besseren Zugriff auf die Dokumentation klinischer Studien, da Teammitglieder von jedem Ort mit Internetverbindung in Echtzeit auf die Dokumente zugreifen können. Dies ist mit der Zunahme entfernter und dezentralisierter klinischer Studien sowie der Notwendigkeit der Zusammenarbeit bei multinationalen Studien zunehmend wichtiger geworden. eTMF-Systeme können mit anderen Systemen für klinische Studien, wie z. B. der elektronischen Datenerfassung (EDC) und Systemen für das klinische Studienmanagement (CTMS), integriert werden, um eine umfassendere und optimierte Lösung für die Verwaltung klinischer Studien zu bieten. Diese Integration ist zu einem Wachstumsfaktor für eTMF-Systeme geworden, da Unternehmen ihre Prozesse und Daten für das Management klinischer Studien vereinheitlichen möchten.
Der allgemeine Trend zu elektronischen Aufzeichnungen im Gesundheitswesen war ebenfalls ein Wachstumsfaktor für eTMF-Systeme. Da immer mehr Unternehmen für die Dokumentation ihrer klinischen Studien auf elektronische Aufzeichnungen umsteigen, sind eTMF-Systeme für die Verwaltung dieser Aufzeichnungen zu einer naheliegenden Wahl geworden.
Einblicke in das Marktsegment Electronic Trial Master File (eTMF)-Systeme
h3
Einblicke in die Komponenten von Electronic Trial Master File (eTMF)-Systemen pDie Marktsegmentierung für Electronic Trial Master File (eTMF)-Systeme, basierend auf Komponenten, umfasst Software und Dienstleistungen. Das Dienstleistungssegment dominierte den Markt im Jahr 2022 und wird im Prognosezeitraum 2022–2030 voraussichtlich das am schnellsten wachsende Segment sein. Ein Wachstumsfaktor für eTMF-Systeme im Dienstleistungssektor ist die Notwendigkeit einer besseren Zusammenarbeit und Zugänglichkeit der Dokumentation klinischer Studien. Dies ist mit der Zunahme von Remote- und dezentralen klinischen Studien sowie der Notwendigkeit der Zusammenarbeit bei multinationalen Studien zunehmend wichtiger geworden. Das eTMF-System von IQVIA wurde entwickelt, um diesem Bedarf gerecht zu werden, indem es eine zentralisierte, Cloud-basierte Plattform für die Verwaltung der Dokumentation klinischer Studien bietet. Das System ermöglicht Teammitgliedern den Echtzeitzugriff auf Dokumente von jedem beliebigen Ort mit Internetverbindung und erleichtert so die Zusammenarbeit und den Zugriff über geografische und zeitzonenübergreifende Bereiche hinweg.
Im Januar 2021 kündigte Parexel, ein führendes Auftragsforschungsinstitut (CRO), die Einführung seiner eTMF-Lösung an, die Kunden dabei unterstützen soll, die Dokumentation klinischer Studien zentral, sicher und konform zu verwalten. Die Lösung ist Teil von Parexels Suite technologiegestützter Dienste für klinische Studien und soll der wachsenden Nachfrage nach eTMF-Lösungen bei biopharmazeutischen Unternehmen gerecht werden.
Einblicke in den Bereitstellungsmodus von Electronic Trial Master File (eTMF)-Systemen
pDie Marktdaten zu Electronic Trial Master File (eTMF)-Systemen wurden nach Bereitstellungsmodus in Cloud-/Web-basiert und vor Ort unterteilt. Das Cloud-/Web-basierte Segment dominierte den Markt im Jahr 2022 und wird im Prognosezeitraum 2022–2030 voraussichtlich das am schnellsten wachsende Segment sein. Die Cloud-basierte Plattform des Systems macht Hardware und Software vor Ort überflüssig, was für Unternehmen zu Kosteneinsparungen führen kann.
Abbildung 1: Markt für Electronic Trial Master File (eTMF)-Systeme nach Bereitstellungsmodus, 2022 2030 (Milliarden USD)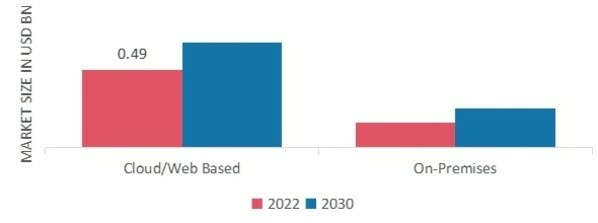
Quelle: Sekundärforschung, Primärforschung, MRFR-Datenbank und Analystenbewertung
Regionale Einblicke in Electronic Trial Master File (eTMF)-Systeme
pNach Regionen sortiert bietet die Studie Markteinblicke für Nordamerika, Europa, den asiatisch-pazifischen Raum und den Rest der Welt. Der nordamerikanische Markt für Electronic Trial Master File (eTMF)-Systeme belief sich im Jahr 2022 auf 0,35 Milliarden US-Dollar und wird im Untersuchungszeitraum voraussichtlich ein signifikantes CAGR-Wachstum aufweisen. Der nordamerikanische Markt wird von Faktoren wie dem zunehmenden Outsourcing klinischer Studien, dem Wachstum der biopharmazeutischen Industrie und dem Bedarf an verbesserten Compliance- und Datensicherheitsmaßnahmen angetrieben. Es wird erwartet, dass der Markt in den kommenden Jahren weiter wächst, angetrieben von Faktoren wie dem Wachstum dezentraler und virtueller Studien, der Einführung cloudbasierter eTMF-Systeme und der steigenden Nachfrage nach Datenanalysen und -erkenntnissen. Darüber hinaus hatte der US-Markt für Electronic Trial Master File (eTMF)-Systeme den größten Marktanteil, und der kanadische Markt für Electronic Trial Master File (eTMF)-Systeme war der am schnellsten wachsende Markt in der Region Nordamerika.
Die wichtigsten im Marktbericht untersuchten Länder sind die USA, Kanada, Deutschland, Frankreich, Großbritannien, Italien, Spanien, China, Japan, Indien, Australien, Südkorea und Brasilien.
Abbildung 2: MARKTANTEIL VON Electronic Trial Master File (eTMF)-Systemen NACH REGION 2022 (%)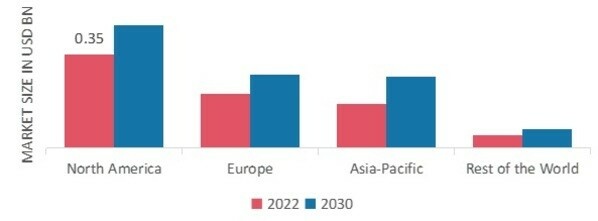
Quelle: Sekundärforschung, Primärforschung, MRFR-Datenbank und Analystenbewertung
Der europäische Markt für Electronic Trial Master File (eTMF)-Systeme nimmt den zweitgrößten Marktanteil ein. Der Markt wird durch die steigende Nachfrage nach natürlichen und biologischen Produkten angetrieben. Der europäische Markt wird durch Faktoren wie die Einhaltung gesetzlicher Vorschriften, die steigende Nachfrage nach Cloud-basierten Lösungen und die Notwendigkeit einer besseren Zusammenarbeit und eines besseren Datenaustauschs zwischen den Beteiligten angetrieben. Es wird erwartet, dass der Markt in den kommenden Jahren weiter wächst, angetrieben von Faktoren wie der Einführung fortschrittlicher Analyse- und KI-Technologien, einem verstärkten Fokus auf Patientenzentrierung und dem Wachstum der Schwellenmärkte in Osteuropa.
Der Markt für Electronic Trial Master File (eTMF)-Systeme im asiatisch-pazifischen Raum wird voraussichtlich von 2022 bis 2030 mit der schnellsten CAGR wachsen. Der Markt wird durch Faktoren wie das Wachstum der biopharmazeutischen Industrie, das zunehmende Outsourcing klinischer Studien und die Einführung fortschrittlicher Technologien angetrieben. Es wird erwartet, dass der Markt in den kommenden Jahren weiter wächst. Treiber hierfür sind Faktoren wie das Wachstum der Schwellenmärkte, die zunehmende Konzentration auf Patientengewinnung und -bindung sowie die Einführung digitaler Gesundheitstechnologien. Der chinesische Markt für Electronic Trial Master File (eTMF)-Systeme hatte den größten Marktanteil, und der indische Markt für Electronic Trial Master File (eTMF)-Systeme war der am schnellsten wachsende Markt im asiatisch-pazifischen Raum.
Wichtige Marktteilnehmer und Wettbewerbseinblicke für Electronic Trial Master File (eTMF)-Systeme
pWichtige Marktteilnehmer investieren viel Geld in Forschung und Entwicklung, um ihr Produktangebot zu erweitern. Dadurch wird das Marktwachstum von Electronic Trial Master File (eTMF)-Systemen weiter steigen. Marktteilnehmer ergreifen zudem eine Reihe strategischer Initiativen, um ihre weltweite Präsenz auszubauen. Wichtige Marktentwicklungen umfassen die Einführung neuer Produkte, vertragliche Vereinbarungen, Fusionen und Übernahmen, erhöhte Investitionen sowie die Zusammenarbeit mit anderen Organisationen. Wettbewerber in der Branche der Electronic Trial Master File (eTMF)-Systeme müssen kostengünstige Produkte anbieten, um in einem zunehmend wettbewerbsorientierten und aufstrebenden Marktumfeld zu expandieren und zu überleben.
Eine der wichtigsten Geschäftsstrategien der Hersteller in der Branche der Electronic Trial Master File (eTMF)-Systeme, um Kunden zu nützen und den Marktsektor zu erweitern, ist die lokale Fertigung zur Senkung der Betriebskosten. In den letzten Jahren hat die Branche der Electronic Trial Master File (eTMF)-Systeme innovative Produkte mit einigen der bedeutendsten Vorteile hervorgebracht. Große Akteure auf dem Markt der Electronic Trial Master File (eTMF)-Systeme wie Aurea, Covance Inc., Mastercontrol Inc., Oracle, Transperfect, Veeva Systems, ePharmaSolutions, Phlex, SureClinical Inc. und andere arbeiten daran, die Marktnachfrage durch Investitionen in Forschung und Entwicklung zu steigern.
Aurea ist ein Softwareunternehmen, das eine Reihe von Produkten und Lösungen für Unternehmen unterschiedlicher Branchen anbietet. Das Portfolio des Unternehmens umfasst Produkte für Customer Experience Management, Enterprise Messaging, Wissensmanagement und Zusammenarbeit. Im Bereich der eTMF-Systeme bietet Aurea das Produkt Aurea Compliance Manager an, eine cloudbasierte Plattform zur Verwaltung der Einhaltung gesetzlicher Vorschriften und der Qualitätskontrollprozesse bei klinischen Studien. Die Lösung umfasst Funktionen für Dokumentenmanagement, Prozessautomatisierung, Prüfpfade und Berichterstellung, die biopharmazeutischen Unternehmen dabei helfen sollen, ihre Compliance- und Qualitätskontrollaktivitäten effizienter und optimierter zu gestalten.
Die eTMF-Lösung von Aurea stammt aus dem Februar 2021. Damals gab das Unternehmen eine Partnerschaft mit dem Biotechnologieunternehmen Halozyme bekannt, um die klinischen Studienprozesse von Halozyme mithilfe des Aurea Compliance Managers zu optimieren. Ziel der Partnerschaft war es, die Studienmanagementprozesse von Halozyme zu verbessern, indem eine zentrale Plattform für die Verwaltung der Aktivitäten zur Einhaltung gesetzlicher Vorschriften bereitgestellt, die Datengenauigkeit und -konsistenz sichergestellt und das mit manuellen Prozessen verbundene Fehler- und Verzögerungsrisiko reduziert wurde. Die Partnerschaft mit Halozyme ist ein Beispiel dafür, wie biopharmazeutische Unternehmen die eTMF-Lösung von Aurea nutzen, um ihre klinischen Studienprozesse zu verbessern und die Einhaltung gesetzlicher Vorschriften sicherzustellen. Da die Nachfrage nach eTMF-Systemen weiter steigt, wird erwartet, dass die Lösung von Aurea eine wichtige Rolle dabei spielt, Unternehmen dabei zu helfen, ihre Compliance- und Qualitätskontrollaktivitäten effizienter und effektiver zu verwalten.Zu den wichtigsten Unternehmen im Markt für elektronische Studienstammdaten (eTMF) gehören:
- Aurea
- Covance Inc.
- Mastercontrol Inc.
- Oracle
- Transperfect
- Veeva Systems
- ePharmaSolutions
- Phlex
- SureClinical Inc.
p
Branchenentwicklungen bei Electronic Trial Master File (eTMF)-Systemen2019 brachte IQVIA, ein Anbieter von Lösungen für klinische Forschung und Gesundheitswesen, seine eTMF-Lösung IQVIA eTMF auf den Markt. Die Lösung umfasst Funktionen für Dokumentenmanagement, Compliance-Tracking und Echtzeit-Reporting.
2019 übernahm Phlex, ein Anbieter von TMF-Managementlösungen, Cunesoft, ein auf Lösungen zur Einhaltung gesetzlicher Vorschriften spezialisiertes deutsches Softwareunternehmen. Durch die Übernahme erweiterte Phlex seine Kompetenzen im Bereich eTMF und Compliance-Management.
2020 übernahm Bioclinica, ein Anbieter von Dienstleistungen für klinische Studien, SMO Clinical Trial Billing Solutions, einen Anbieter von eTMF-Lösungen. Durch die Übernahme erweiterte Bioclinica sein Angebot in eTMF- und Finanzmanagementlösungen für klinische Studien.
Marktsegmentierung für Electronic Trial Master File (eTMF)-Systeme
h3
Ausblick auf Komponenten von Electronic Trial Master File (eTMF)-Systemen ul
Software Dienste h3
Ausblick auf Bereitstellungsmodi von Electronic Trial Master File (eTMF)-Systemen ul
Cloud-/Webbasiert On-Premise h3
Ausblick auf Endnutzer von Electronic Trial Master File (eTMF)-Systemen ul
Pharma- und Biotechnologieunternehmen Auftragsforschungsinstitute Sonstige h3
Regionale Bereitstellung von Electronic Trial Master File (eTMF)-Systemen Ausblick ul
- Asien-Pazifik
- Restlicher Asien-Pazifik-Raum
















