
Globaler Marktüberblick für Electronic Trial Master File (eTMF)-Systeme
Laut MRFR-Analyse wurde die Marktgröße für Electronic Trial Master File Systems im Jahr 2024 auf 1,02 (Milliarden US-Dollar) geschätzt. Es wird erwartet, dass der Markt für Electronic Trial Master File Systems von 1,16 (Milliarden US-Dollar) im Jahr 2025 auf 3,81 (Milliarden US-Dollar) bis 2034 wachsen wird, wobei eine CAGR (Wachstumsrate) im Prognosezeitraum voraussichtlich bei etwa 14,12 % liegen wird (2025 - 2034). Die Einhaltung gesetzlicher Vorschriften, Effizienz und Kosteneinsparungen sowie die zunehmende Einführung elektronischer Aufzeichnungen sind die wichtigsten Markttreiber, die das Marktwachstum fördern
Quelle: Sekundärforschung, Primärforschung, MRFR-Datenbank und Analystenbewertung
Markttrends für elektronische Trial-Master-File-Systeme (eTMF)
- Zunehmende Einführung elektronischer Aufzeichnungen zur Ankurbelung des Marktwachstums
Die Pharma- und Biotech-Branche ist stark reguliert, und eTMF-Systeme bieten Unternehmen die Möglichkeit, ihre Dokumentation zu klinischen Studien in Übereinstimmung mit Vorschriften wie 21 CFR Part 11 zu verwalten. Dies war ein bedeutender Wachstumsfaktor für eTMF-Systeme, da Unternehmen versuchen, das Risiko von Strafen bei Nichteinhaltung zu vermeiden und ihre behördlichen Meldeprozesse zu optimieren.
eTMF-Systeme können die Effizienz klinischer Studien verbessern, indem sie den Zeit- und Arbeitsaufwand für die Verwaltung der Studiendokumentation reduzieren. Dies kann zu Kosteneinsparungen für Unternehmen führen, da sie weniger Ressourcen für die Verwaltung ihrer Versuche benötigen. Beispielsweise ergab eine Studie des Tufts Center for the Study of Drug Development, dass eTMF-Systeme den Zeitaufwand für die Fertigstellung der Dokumentation klinischer Studien um bis zu 10 % reduzieren können.
eTMF-Systeme ermöglichen eine bessere Zusammenarbeit und Zugänglichkeit der Dokumentation klinischer Studien, da Teammitglieder von jedem Ort mit Internetverbindung aus in Echtzeit auf Dokumente zugreifen können. Dies ist mit der Zunahme entfernter und dezentraler klinischer Studien sowie der Notwendigkeit der Zusammenarbeit bei multinationalen Studien immer wichtiger geworden. eTMF-Systeme können in andere Systeme für klinische Studien integriert werden, wie z. B. elektronische Datenerfassung (EDC) und Managementsysteme für klinische Studien (CTMS), um eine umfassendere und optimierte Lösung für die Verwaltung klinischer Studien bereitzustellen. Diese Integration ist zu einem Wachstumsfaktor für eTMF-Systeme geworden, da Unternehmen ihre Prozesse und Daten für das Management klinischer Studien vereinheitlichen möchten.
Der allgemeine Trend zu elektronischen Akten im Gesundheitswesen war auch ein Wachstumsfaktor für eTMF-Systeme. Da immer mehr Unternehmen für die Dokumentation ihrer klinischen Studien auf elektronische Aufzeichnungen umsteigen, sind eTMF-Systeme eine natürliche Wahl für die Verwaltung dieser Aufzeichnungen geworden.
Einblicke in das Marktsegment von Electronic Trial Master File (eTMF)-Systemen
Einblicke in Systemkomponenten des Electronic Trial Master File (eTMF)
Die Marktsegmentierung für Electronic Trial Master File (eTMF)-Systeme umfasst nach Komponenten Software und Dienstleistungen. Das Dienstleistungssegment dominierte den Markt im Jahr 2022 und wird im Prognosezeitraum 2022–2030 voraussichtlich das am schnellsten wachsende Segment sein. Ein Wachstumsfaktor für eTMF-Systeme im Dienstleistungsbereich ist die Notwendigkeit einer besseren Zusammenarbeit und Zugänglichkeit der Dokumentation klinischer Studien. Dies ist mit der Zunahme entfernter und dezentraler klinischer Studien sowie der Notwendigkeit der Zusammenarbeit bei multinationalen Studien immer wichtiger geworden. Das eTMF-System von IQVIA ist darauf ausgelegt, diesem Bedarf gerecht zu werden, indem es eine zentralisierte, cloudbasierte Plattform für die Verwaltung der Dokumentation klinischer Studien bereitstellt. Das System ermöglicht Teammitgliedern den Zugriff auf Dokumente in Echtzeit von überall mit einer Internetverbindung und erleichtert so die Zusammenarbeit und den Zugriff über Regionen und Zeitzonen hinweg.
Im Januar 2021 em kündigte Parexel, ein führendes Auftragsforschungsinstitut (CRO), die Einführung seiner eTMF-Lösung an, die Kunden dabei helfen soll, die Dokumentation klinischer Studien zentral, sicher und konform zu verwalten. Die Lösung ist Teil der Reihe technologiegestützter Dienstleistungen von Parexel für klinische Studien und soll der wachsenden Nachfrage biopharmazeutischer Unternehmen nach eTMF-Lösungen gerecht werden.
Einblicke in den Bereitstellungsmodus von Electronic Trial Master File (eTMF)-Systemen
Die Marktdaten für Electronic Trial Master File (eTMF)-Systeme wurden je nach Bereitstellungsmodus in cloud-/webbasiert und lokal unterteilt. Das cloud-/webbasierte Segment dominierte den Markt im Jahr 2022 und dürfte im Prognosezeitraum 2022–2030 das am schnellsten wachsende Segment sein. Die cloudbasierte Plattform des Systems macht lokale Hardware und Software überflüssig, was zu Kosteneinsparungen für Unternehmen führen kann.
Abbildung 1 Markt für Electronic Trial Master File (eTMF)-Systeme, nach Bereitstellungsmodus, 2022 2030 (Milliarden USD)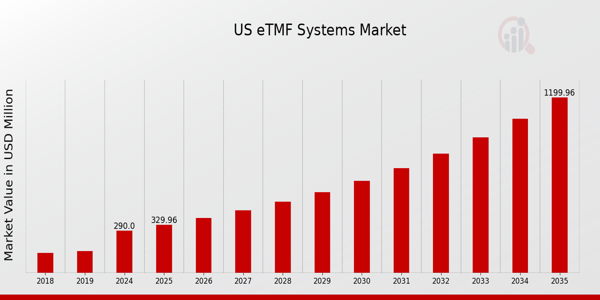
Quelle: Sekundärforschung, Primärforschung, MRFR-Datenbank und Analystenbewertung
Electronic Trial Master File (eTMF) Systems Regional Insights
Nach Regionen bietet die Studie Markteinblicke in Nordamerika, Europa, den asiatisch-pazifischen Raum und den Rest der Welt. Der nordamerikanische Markt für Electronic Trial Master File (eTMF)-Systeme hatte im Jahr 2022 einen Wert von 0,35 Milliarden US-Dollar und wird im Untersuchungszeitraum voraussichtlich ein deutliches CAGR-Wachstum verzeichnen. Der nordamerikanische Markt wird durch Faktoren wie die zunehmende Auslagerung klinischer Studien, das Wachstum in der biopharmazeutischen Industrie und die Notwendigkeit besserer Compliance- und Datensicherheitsmaßnahmen angetrieben. Es wird erwartet, dass der Markt in den kommenden Jahren weiter wachsen wird, angetrieben durch Faktoren wie das Wachstum dezentraler und virtueller Studien, die Einführung cloudbasierter eTMF-Systeme und die steigende Nachfrage nach Datenanalysen und Erkenntnissen. Darüber hinaus hielt der US-amerikanische Markt für Electronic Trial Master File (eTMF)-Systeme den größten Marktanteil, und der kanadische Markt für Electronic Trial Master File (eTMF)-Systeme war der am schnellsten wachsende Markt in der nordamerikanischen Region.
Darüber hinaus sind die wichtigsten im Marktbericht untersuchten Länder die USA, Kanada, Deutschland, Frankreich, Großbritannien, Italien, Spanien, China, Japan, Indien, Australien, Südkorea und Brasilien.
Abbildung 2 Marktanteil von Electronic Trial Master File (eTMF)-Systemen nach Region 2022 (%)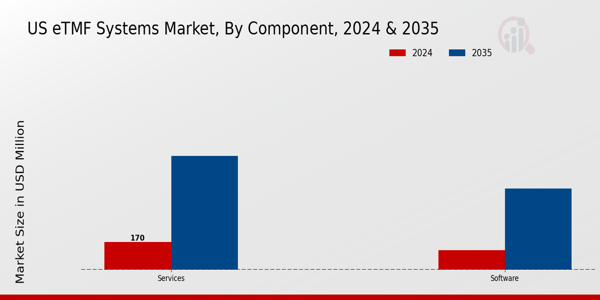
Quelle: Sekundärforschung, Primärforschung, MRFR-Datenbank und Analystenbewertung
Der europäische Markt für Electronic Trial Master File (eTMF) hat den zweitgrößten Marktanteil. Der Markt wird durch die steigende Nachfrage nach natürlichen und biologischen Produkten angetrieben. Der europäische Markt wird von Faktoren wie der Einhaltung gesetzlicher Vorschriften, der steigenden Nachfrage nach Cloud-basierten Lösungen und der Notwendigkeit einer besseren Zusammenarbeit und eines besseren Datenaustauschs zwischen den Beteiligten bestimmt. Es wird erwartet, dass der Markt in den kommenden Jahren weiter wachsen wird, angetrieben durch Faktoren wie die Einführung fortschrittlicher Analyse- und KI-Technologien, einen verstärkten Fokus auf Patientenzentrierung und das Wachstum aufstrebender Märkte in Osteuropa.
Der Markt für eTMF-Systeme (Electronic Trial Master File) im asiatisch-pazifischen Raum wird voraussichtlich von 2022 bis 2030 mit der schnellsten jährlichen Wachstumsrate wachsen. Der Markt wird durch Faktoren wie das Wachstum der biopharmazeutischen Industrie, die zunehmende Auslagerung klinischer Studien und die Einführung fortschrittlicher Technologien angetrieben. Es wird erwartet, dass der Markt in den kommenden Jahren weiter wachsen wird, angetrieben durch Faktoren wie das Wachstum der Schwellenländer, den zunehmenden Fokus auf Patientenrekrutierung und -bindung sowie die Einführung digitaler Gesundheitstechnologien. Darüber hinaus hielt der chinesische Markt für Electronic Trial Master File (eTMF)-Systeme den größten Marktanteil, und der indische Markt für Electronic Trial Master File (eTMF)-Systeme war der am schnellsten wachsende Markt im asiatisch-pazifischen Raum.
Electronic Trial Master File (eTMF)-Systeme Wichtige Marktteilnehmer Wettbewerbseinblicke
Große Marktteilnehmer geben viel Geld für Forschung und Entwicklung aus, um ihre Produktlinien zu erweitern, was dazu beitragen wird, dass der Markt für Electronic Trial Master File (eTMF)-Systeme noch weiter wächst. Marktteilnehmer ergreifen außerdem eine Reihe strategischer Initiativen, um ihre weltweite Präsenz auszubauen, mit wichtigen Marktentwicklungen wie der Einführung neuer Produkte, vertraglichen Vereinbarungen, Fusionen und Übernahmen, erhöhten Investitionen und der Zusammenarbeit mit anderen Organisationen. Wettbewerber in der Branche der Electronic Trial Master File (eTMF)-Systeme müssen kostengünstige Artikel anbieten, um in einem zunehmend wettbewerbsintensiven und wachsenden Marktumfeld zu expandieren und zu bestehen.
Eine der wichtigsten Geschäftsstrategien der Hersteller in der Branche der elektronischen Trial-Master-File-Systeme (eTMF) zum Nutzen der Kunden und zur Erweiterung des Marktsektors besteht darin, vor Ort zu produzieren und so die Betriebskosten zu senken. In den letzten Jahren hat die Branche der Electronic Trial Master File (eTMF)-Systeme innovative Produkte mit einigen der bedeutendsten Vorteile bereitgestellt. Die wichtigsten Marktteilnehmer von Electronic Trial Master File (eTMF)-Systemen wie Aurea, Covance Inc., Mastercontrol Inc., Oracle, Transperfect, Veeva Systems, ePharmaSolutions, Phlex, SureClinical Inc. und andere arbeiten daran, die Marktnachfrage durch Investitionen in Forschungs- und Entwicklungsaktivitäten zu erweitern.
Aurea ist ein Softwareunternehmen, das eine Reihe von Produkten und Lösungen für Unternehmen verschiedener Branchen anbietet. Das Portfolio des Unternehmens umfasst Produkte für Customer Experience Management, Enterprise Messaging, Wissensmanagement und Zusammenarbeit. In Bezug auf eTMF-Systeme bietet Aurea ein Produkt namens Aurea Compliance Manager an, eine cloudbasierte Plattform zur Verwaltung der Einhaltung gesetzlicher Vorschriften und Qualitätskontrollprozesse in klinischen Studien. Die Lösung umfasst Funktionen für Dokumentenmanagement, Prozessautomatisierung, Audit-Trails und Reporting, die alle darauf ausgelegt sind, biopharmazeutischen Unternehmen dabei zu helfen, ihre Compliance- und Qualitätskontrollaktivitäten effizienter und rationaler zu verwalten. Die eTMF-Lösung von Aurea stammt aus dem Februar 2021, als das Unternehmen bekannt gab, dass es eine Partnerschaft mit Halozyme, einem Biotechnologieunternehmen, eingegangen ist, um die Prozesse für klinische Studien von Halozyme mithilfe des Aurea Compliance Managers zu optimieren. Ziel der Partnerschaft war es, die Studienmanagementprozesse von Halozyme zu verbessern, indem eine zentrale Plattform für die Verwaltung der Aktivitäten zur Einhaltung gesetzlicher Vorschriften bereitgestellt, die Genauigkeit und Konsistenz der Daten sichergestellt und das Risiko von Fehlern und Verzögerungen im Zusammenhang mit manuellen Prozessen verringert wird. Die Partnerschaft mit Halozyme ist ein Beispiel dafür, wie die eTMF-Lösung von Aurea von biopharmazeutischen Unternehmen genutzt wird, um ihre Prozesse für klinische Studien zu verbessern und die Einhaltung gesetzlicher Vorschriften sicherzustellen. Da die Nachfrage nach eTMF-Systemen weiter wächst, wird die Lösung von Aurea voraussichtlich eine wichtige Rolle dabei spielen, Unternehmen dabei zu helfen, ihre Compliance- und Qualitätskontrollaktivitäten effizienter und effektiver zu verwalten.
Covance Inc ist ein Auftragsforschungsinstitut (Contract Research Organization, CRO), das eine Reihe von Dienstleistungen für biopharmazeutische und medizinische Geräteunternehmen anbietet, darunter klinische Entwicklung, Labortests und Kommerzialisierungsdienste. Das Unternehmen ist in über 60 Co. tätiguntrys und hat eine Belegschaft von mehr als 50.000 Mitarbeitern. In Bezug auf eTMF-Systeme bietet Covance ein Produkt namens Xcellerate® eTMF an, eine cloudbasierte Plattform zur gesetzeskonformen und sicheren Verwaltung und Speicherung von Dokumenten zu klinischen Studien. Die Lösung umfasst Funktionen wie Dokumentenmanagement, Prüfprotokolle und Echtzeitberichte, die alle darauf ausgelegt sind, Sponsoren klinischer Studien dabei zu helfen, ihre Studiendokumentation effizienter und effektiver zu verwalten. Eine aktuelle Nachricht im Zusammenhang mit der eTMF-Lösung von Covance stammt aus dem Oktober 2020, als das Unternehmen bekannt gab, dass es eine neue Version von Xcellerate® eTMF auf den Markt gebracht hat. Die neue Version umfasste mehrere Verbesserungen, wie z. B. verbesserte Funktionen zur Dokumentenverwaltung, erweiterte Prüfpfade und Echtzeitüberwachung der Vollständigkeit und Compliance von Dokumenten. Die neue Version umfasste auch Integrationen mit anderen Covance-Produkten, wie z. B. Xcellerate® Monitoring, einer risikobasierten Überwachungslösung.
Zu den wichtigsten Unternehmen im Markt für Electronic Trial Master File (eTMF)-Systeme gehören
- Aurea
- Covance Inc.
- Mastercontrol Inc.
- Oracle
- Transperfekt
- Veeva-Systeme
- ePharmaSolutions
- Phlex
- SureClinical Inc.
Entwicklungen in der Electronic Trial Master File (eTMF)-Systembranche
Im Jahr 2019 em brachte IQVIA, ein Anbieter von Lösungen für klinische Forschung und Gesundheitswesen, seine eTMF-Lösung IQVIA eTMF auf den Markt. Die Lösung umfasst Funktionen für Dokumentenmanagement, Compliance-Verfolgung und Echtzeit-Berichterstellung.
Im Jahr 2019 em erwarb Phlex, ein Anbieter von TMF-Managementlösungen, im Jahr 2019 Cunesoft, ein in Deutschland ansässiges Softwareunternehmen, das sich auf Lösungen zur Einhaltung gesetzlicher Vorschriften spezialisiert hat. Die Übernahme erweiterte die Fähigkeiten von Phlex im Bereich eTMF und Management zur Einhaltung gesetzlicher Vorschriften.
Im Jahr 2020 em erwarb Bioclinica, ein Anbieter von Dienstleistungen für klinische Studien, im Jahr 2020 SMO Clinical Trial Billing Solutions, einen Anbieter von eTMF-Lösungen. Durch die Übernahme erweiterte Bioclinica sein Angebot an eTMF- und Finanzmanagementlösungen für klinische Studien.
Marktsegmentierung für Electronic Trial Master File (eTMF)-Systeme
Electronic Trial Master File (eTMF) Systems Component Outlook
- Software
- Dienste
Electronic Trial Master File (eTMF) Systems Deployment Mode Outlook
- Cloud-/webbasiert
- Vor Ort
Electronic Trial Master File (eTMF) Systems End User Outlook
- Pharma- und Biotechnologieunternehmen
- Auftragsforschungsorganisationen
- Andere
Electronic Trial Master File (eTMF) Systems Regional Outlook
- Nordamerika
- USA
- Kanada
- Europa
- Deutschland
- Frankreich
- Großbritannien
- Italien
- Spanien
- Restliches Europa
- Asien-Pazifik
- China
- Japan
- Indien
- Australien
- Südkorea
- Australien
- Restlicher Asien-Pazifik-Raum
- Rest der Welt
- Naher Osten
- Afrika
- Lateinamerika
FAQs
What is the projected market size of the US eTMF Systems Market in 2024?
The US eTMF Systems Market is projected to be valued at 290.0 million USD in 2024.
What is the expected market valuation for the US eTMF Systems Market by 2035?
By 2035, the US eTMF Systems Market is expected to reach a valuation of 1200.0 million USD.
What is the expected CAGR for the US eTMF Systems Market from 2025 to 2035?
The US eTMF Systems Market is expected to grow at a CAGR of 13.781% from 2025 to 2035.
What are the key components of the US eTMF Systems Market, and their market value in 2024?
The key components are Software valued at 120.0 million USD and Services valued at 170.0 million USD in 2024.
What will the market value of the Software component in the US eTMF Systems Market be by 2035?
The Software component of the US eTMF Systems Market is expected to be valued at 500.0 million USD by 2035.
What will the market value of the Services component in the US eTMF Systems Market be by 2035?
The Services component is projected to reach a valuation of 700.0 million USD in 2035.
Who are some of the major players in the US eTMF Systems Market?
Major players include SAP, Cognizant, Wipro, Oracle, and Veeva Systems among others.
What opportunities are driving growth in the US eTMF Systems Market?
Opportunities are being driven by increasing automation and regulatory requirements in clinical trials.
How are emerging trends impacting the US eTMF Systems Market?
Emerging trends such as AI integration and data analytics are significantly enhancing efficiency in the market.
What challenges does the US eTMF Systems Market currently face?
Challenges include data security concerns and the need for compliance with evolving regulations.
Bitte füllen Sie das folgende Formular aus, um ein kostenloses Muster dieses Berichts zu erhalten
Customer Stories

“This is really good guys. Excellent work on a tight deadline. I will continue to use you going forward and recommend you to others. Nice job”

“Thanks. It’s been a pleasure working with you, please use me as reference with any other Intel employees.”

“Thanks for sending the report it gives us a good global view of the Betaïne market.”

“Thank you, this will be very helpful for OQS.”

“We found the report very insightful! we found your research firm very helpful. I'm sending this email to secure our future business.”

“I am very pleased with how market segments have been defined in a relevant way for my purposes (such as "Portable Freezers & refrigerators" and "last-mile"). In general the report is well structured. Thanks very much for your efforts.”

“I have been reading the first document or the study, ,the Global HVAC and FP market report 2021 till 2026. Must say, good info! I have not gone in depth at all parts, but got a good indication of the data inside!”

“We got the report in time, we really thank you for your support in this process. I also thank to all of your team as they did a great job.”

