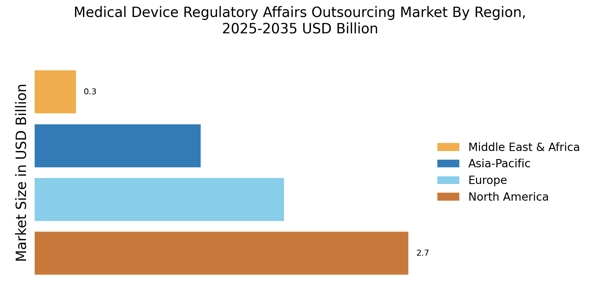
医療機器規制業務アウトソーシング市場は、規制要件の複雑化と迅速な市場アクセスの必要性によって推進される動的な競争環境が特徴です。Medpace(米国)、PAREXEL(米国)、ICON plc(アイルランド)などの主要プレーヤーは、規制業務、臨床試験、市場アクセス戦略における広範な専門知識を活用するために戦略的に位置づけられています。Medpace(米国)は、戦略的パートナーシップを通じてグローバルな足跡を強化することに注力しており、PAREXEL(米国)は規制コンサルティングサービスにおける革新を強調しています。ICON plc(アイルランド)は、規制プロセスを効率化するために先進技術を統合するデジタルトランスフォーメーションアプローチを採用しています。これらの戦略は、運営効率を向上させるだけでなく、規制の変化に対する機敏さと応答性を優先する競争環境を形成しています。
ビジネス戦略に関して、企業は地域の規制フレームワークにより適合させるために、オペレーションのローカライズを進めており、サプライチェーンの最適化を図っています。市場は中程度に分散しているようで、大手多国籍企業と専門企業が混在しています。この構造は、多様なサービスの提供を可能にし、クライアントが特定の規制ニーズに最も適したパートナーを選択できるようにしています。これらの主要プレーヤーの集合的な影響は、革新と適応性が最も重要な競争環境を育んでいます。
2025年8月、Medpace(米国)は、規制コンプライアンスプロセスを強化することを目的としたAI駆動のプラットフォームを開発するために、主要なテクノロジー企業との戦略的パートナーシップを発表しました。この取り組みにより、規制提出に必要な時間が大幅に短縮され、全体的な製品開発のタイムラインが加速されると期待されています。規制業務へのAIの統合は、Medpaceを先進的なリーダーとして位置づけるだけでなく、デジタル化に向けた業界全体のトレンドを反映しています。
2025年9月、PAREXEL(米国)は、規制提出においてますます重要となる実世界の証拠生成に焦点を当てた新しいサービススイートを発表しました。この動きは、複雑な規制環境におけるクライアントの進化するニーズに対応する包括的なソリューションを提供するというPAREXELのコミットメントを強調しています。サービス提供を強化することで、PAREXELは市場での地位を固め、規制業務におけるデータ駆動の洞察に対する高まる需要に効果的に応えることを目指しています。
2025年7月、ICON plc(アイルランド)は、欧州市場アクセス戦略に特化したニッチコンサルティング会社を買収することで、規制業務の能力を拡大しました。この買収は、ICONのサービスポートフォリオを広げるだけでなく、欧州の複雑な規制環境をナビゲートする能力を強化します。このような戦略的な動きは、市場における統合の傾向を示しており、企業が競争力を維持するために専門知識とサービス提供を強化しようとしています。
2025年10月現在、医療機器規制業務アウトソーシング市場の競争トレンドは、デジタル化、持続可能性、人工知能の統合によってますます定義されています。戦略的アライアンスがますます普及しており、企業はリソースと専門知識を集めて複雑な規制の課題に取り組むことができるようになっています。今後、競争の差別化は、従来の価格競争から革新、技術の進歩、サプライチェーンの信頼性に焦点を当てたものに進化する可能性が高いです。このシフトは、企業が市場での位置づけを再定義し、規制の要求に対する機敏さと応答性の重要性を強調することになるでしょう。