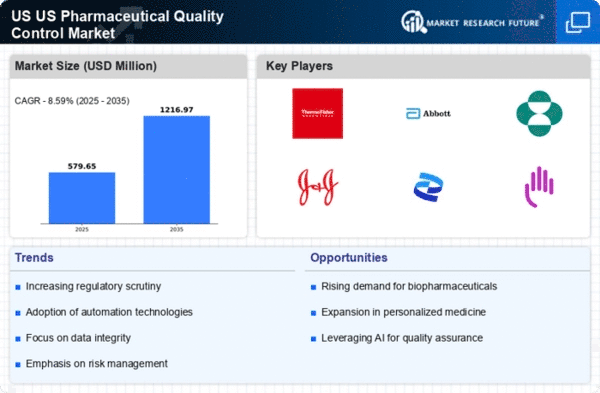
Überblick über den globalen Markt für pharmazeutische Qualitätskontrolle
Die Größe des Marktes für pharmazeutische Qualitätskontrolle wurde im Jahr 2022 auf 4,1 Milliarden US-Dollar geschätzt. Der Markt für pharmazeutische Qualitätskontrolle wird Prognosen zufolge von 4,6 Milliarden US-Dollar im Jahr 2023 auf 11,5 Milliarden US-Dollar im Jahr 2032 wachsen und im Prognosezeitraum (2024–2032) eine durchschnittliche jährliche Wachstumsrate (CAGR) von 12,10 % aufweisen. Die Arzneimittelproduktion wird teurer, und die zunehmende Notwendigkeit, regulatorische Vorschriften einzuhalten, sind die wichtigsten Markttreiber, die das Marktwachstum fördern.
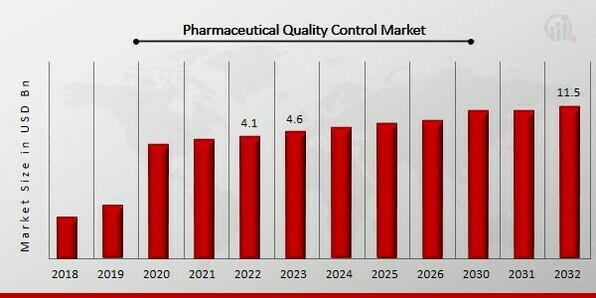
Quelle: Sekundärforschung, Primärforschung, MRFR-Datenbank und Analystenbewertung
Markttrends für pharmazeutische Qualitätskontrolle
- Steigende Kosten für die Arzneimittelherstellung treiben das Marktwachstum voran
In der Pharmabranche machen die Herstellungskosten einen erheblichen Teil der Gesamtkosten eines Unternehmens aus. Auch die Entwicklungskosten eines neuen Medikaments steigen stetig. Der voraussichtliche Investitionsbedarf für die erfolgreiche Kommerzialisierung einer im Labor entwickelten Idee beträgt 2 Milliarden US-Dollar. Arzneimittel mit einem erkennbaren Markennamen können bis zu 27–30 % des Umsatzes kosten. Einerseits erhöhen Pharmaunternehmen ihre FE-Ausgaben, um mehr Produkte herzustellen, aber die Produktivität ihrer FE-Investitionen nimmt im Vergleich zur Anzahl der Arzneimittel, die jedes Jahr auf den Markt kommen, ab, was sich auf einen erheblichen Teil ihrer Gesamtkostenstruktur auswirkt. Viele Pharma- und Biotech-Industrien konzentrieren sich aufgrund der steigenden Nachfrage nach einer Senkung der Gesamtprozesskosten darauf, ihre Prozesse mit Hilfe von Qualitätsmanagementsystemen zu vereinfachen.
Pharmaunternehmen unterliegen einer starken Regulierung, da Medikamente, Medizinprodukte und andere Arzneimittel einen direkten Einfluss auf die Gesundheit und das Wohlbefinden der Verbraucher haben. Um ihre Waren verkaufen zu können, müssen Hersteller eine Reihe von Qualitätskriterien einhalten. Kleine und mittlere Pharmaunternehmen konzentrieren sich aufgrund der rasanten Expansion der Pharmaindustrie auf die Einhaltung von Gesetzen, um bessere Produkte herzustellen und ihre Wettbewerbsfähigkeit auf dem Markt aufrechtzuerhalten. Die Food and Drug Administration (FDA) reguliert den US-Markt, wohin die meisten Unternehmen in Entwicklungsländern wie China und Indien ihre Waren versenden. Die FDA prüft die Einrichtungen und Betriebsmethoden aller pharmazeutischen Produktionsaktivitäten in den USA sowie die Auslandsaktivitäten von Unternehmen, die ihre Waren routinemäßig in den USA verkaufen. Daher müssen diese Einrichtungen und ihre Prozesse die aktuellen guten Herstellungspraktiken (cGMP) der FDA befolgen. Um ihre Waren herzustellen und zu vermarkten, müssen Unternehmen außerdem die Bestimmungen der International Organization for Standardization (ISO), 21 CFR Part 211 und ICH Guideline Q10 einhalten. Aufgrund der zunehmenden Bedeutung regulatorischer Anforderungen und des wachsenden Marktes sind Hersteller bestrebt, Qualitätsmanagementsysteme einzuführen.
Die Hauptgründe, die den Markt für pharmazeutische Qualitätskontrollen vorantreiben, sind die wachsende Zahl akkreditierter klinischer Labore, die zunehmende Akzeptanz von Qualitätskontrollen Dritter und die wachsende Präferenz für externe Hilfe bei der Qualitätsbewertung. Die Zahl der durchgeführten Labortests hat aufgrund der weltweit steigenden Prävalenz verschiedener Krankheiten zugenommen. Sowohl der öffentliche als auch der private Sektor erhöhen die Zahl der Labore, um dieser Anforderung gerecht zu werden. Klinische Labore müssen in den meisten Ländern eine Akkreditierung von Regulierungsorganisationen wie der International Organization for Standardization und anderen vergleichbaren Standards erhalten, um diagnostische Tests durchführen zu können. Die zuständigen Behörden bewerten die Kompetenz und das Qualitätssystem eines Labors im Vergleich zu vorgegebenen Standards während des Akkreditierungsverfahrens und steigern so den Umsatz auf dem Markt für pharmazeutische Qualitätskontrolle.
Einblicke in das Marktsegment für pharmazeutische Qualitätskontrolle
Produkteinblicke in die pharmazeutische Qualitätskontrolle
Die Marktsegmentierung für pharmazeutische Qualitätskontrolle umfasst nach Produkten Verbrauchsmaterialien, Instrumente und Dienstleistungen. Das Segment Verbrauchsmaterialien dominierte den Markt im Jahr 2022. Die in der Produktion verwendeten Haupthilfsstoffe sind Verbrauchsmaterialien. Verbrauchsmaterialien können in drei Kategorien eingeteilt werden: solche, die keinen Einfluss auf die Qualität haben, solche, die einen Einfluss haben, und solche, die einen direkten Einfluss haben. Den Prognosen zufolge wird der Dienstleistungssektor am schnellsten wachsen. Darüber hinaus liegt der höchste Marktanteil für pharmazeutische Qualität und Kontrolle im Instrumentenbereich.
Einblicke in die Art der Analyse der pharmazeutischen Qualitätskontrolle
Die Marktsegmentierung für pharmazeutische Qualitätskontrolle, basierend auf dem Analysetyp, umfasst Sterilitätstests, Keimbelastungstests, Endotoxintests, Stabilitätstests sowie extrahierbare und biochemische Tests. Prüfung auf auslaugbare Stoffe, Prüfung von Rohstoffen und andere. Das Segment Keimzahltests dominierte den Markt im Jahr 2022. Anaerobe Keimzahltests, aerobe Keimzahltests, Schimmelpilzzahltests, In-vitro, Sporenzahltests, Endotoxintests, LAL und andere sind die verschiedenen Kategorien, in die Keimzahltests unterteilt werden. Die Bakterienpopulation in einer Probe wird mithilfe eines aeroben Zähltests analysiert. Es hilft dabei, die Qualität und den Grad der Verschlechterung des Produkts anzuzeigen. Die Wundkultur, auch anaerober Zähltest genannt, wird ohne den Einsatz von Sauerstoff durchgeführt.
Getestete Einblicke in pharmazeutische Qualitätskontrollprodukte
Die Marktsegmentierung für pharmazeutische Qualitätskontrolle, basierend auf den getesteten Produkten, umfasst Impfstoffe, Plasmaprodukte und Medikamente. Das Segment Impfstoffe dominierte im Jahr 2022 den Markt für pharmazeutische Qualitätskontrolle. Es ist wirklich wichtig, wesentliche Optionen für die Qualitätskontrolle und Impfstoffproduktion zu finden. Insgesamt wird das Untersegment der Arzneimittel voraussichtlich am schnellsten wachsen.
Abbildung 1: Markt für pharmazeutische Qualitätskontrolle, nach getesteten Produkten, 2023 2032 (Milliarden USD)
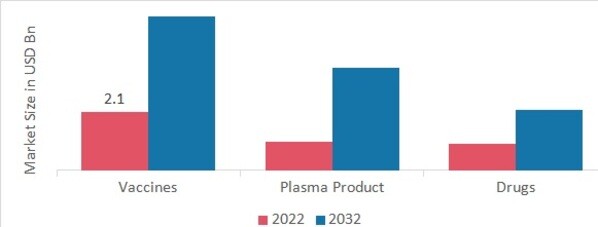
Quelle: Sekundärforschung, Primärforschung, MRFR-Datenbank und Analystenbewertung
Regionale Einblicke in die pharmazeutische Qualitätskontrolle
Nach Regionen bietet die Studie Markteinblicke in Nordamerika, Europa, den asiatisch-pazifischen Raum und den Rest der Welt. Der nordamerikanische Markt für pharmazeutische Qualitätskontrolle dominierte diesen Markt im Jahr 2022 (45,80 %). Dies ist auf die entwickelten Gesundheitssysteme in den Vereinigten Staaten und Kanada, die Präsenz zahlreicher führender Hersteller von Produkten zur molekularen Qualitätskontrolle in der Region und die Zugänglichkeit modernster Technologien in der Region zurückzuführen. Darüber hinaus hatte der US-amerikanische Markt für pharmazeutische Qualitätskontrolle den größten Marktanteil und der kanadische Markt für pharmazeutische Qualitätskontrolle war der am schnellsten wachsende Markt in der Region Nordamerika.
Darüber hinaus sind die wichtigsten im Marktbericht untersuchten Länder die USA, Kanada, Deutschland, Frankreich, das Vereinigte Königreich, Italien, Spanien, China, Japan, Indien, Australien, Südkorea und Brasilien.
Abbildung 2: MARKTANTEIL DER PHARMAZEUTISCHEN QUALITÄTSKONTROLLE NACH REGIONEN 2023 (Milliarden USD)
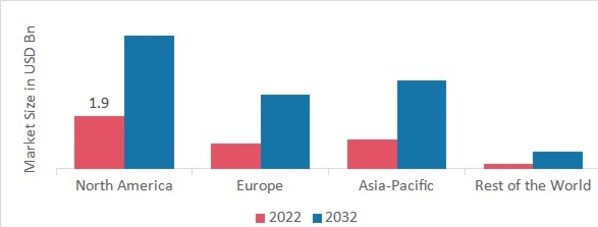
Quelle: Sekundärforschung, Primärforschung, MRFR-Datenbank und Analystenbewertung
Der Markt für pharmazeutische Qualitätskontrolle in Europa hatte im Jahr 2022 einen guten Marktanteil. Im Prognosezeitraum wird erwartet, dass erhebliche Investitionen in Forschung und Entwicklung für die Pharmaindustrie den Markt für pharmazeutische Qualitätskontrolle in Europa ankurbeln werden. Laut der European Federation of Pharmaceutical Industries and Associations (EFPIA) gab das forschungsbasierte Pharmaunternehmen im Jahr 2017 schätzungsweise 35.200 Millionen Euro für Forschung und Entwicklung in Europa aus. Darüber hinaus hatte der deutsche Markt für pharmazeutische Qualitätskontrolle den größten Marktanteil und der britische Markt für pharmazeutische Qualitätskontrolle war der am schnellsten wachsende Markt in der europäischen Region.
Der Markt für pharmazeutische Qualitätskontrolle im asiatisch-pazifischen Raum wird voraussichtlich von 2024 bis 2032 ein deutliches Wachstum verzeichnen. Eine große Anzahl von Pharmaunternehmen ist für die Expansion dieses Marktes verantwortlich. Die größten Hersteller von Generika und Biopharmazeutika sind in der Pharmaindustrie Chinas und Indiens zu finden, und die Mehrheit der Unternehmen, die Qualitätsmanagementsysteme anbieten, konzentriert sich darauf, Marktanteile in diesen wichtigen Pharmamärkten zu gewinnen. Darüber hinaus hielt der chinesische Markt für pharmazeutische Qualitätskontrolle den größten Marktanteil und der indische Markt für pharmazeutische Qualitätskontrolle war der am schnellsten wachsende Markt im asiatisch-pazifischen Raum.
Pharmazeutische Qualitätskontrolle – wichtige Marktteilnehmer Wettbewerbseinblicke
Führende Marktteilnehmer investieren stark in Forschung und Entwicklung, um ihre Produktlinien zu erweitern, was dazu beitragen wird, dass der Markt für pharmazeutische Qualitätskontrolle noch stärker wächst. Marktteilnehmer unternehmen außerdem eine Vielzahl strategischer Aktivitäten, um ihre Präsenz zu erweitern. Zu wichtigen Marktentwicklungen gehören die Einführung neuer Produkte, vertragliche Vereinbarungen, Fusionen und Übernahmen, höhere Investitionen und die Zusammenarbeit mit anderen Organisationen. Um in einem wettbewerbsintensiveren und steigenden Marktklima zu expandieren und zu bestehen, muss die pharmazeutische Qualitätskontrollbranche kostengünstige Artikel anbieten.
Die Herstellung vor Ort zur Minimierung der Betriebskosten ist eine der wichtigsten Geschäftstaktiken, die Hersteller in der pharmazeutischen Qualitätskontrollbranche einsetzen, um Kunden zu helfen und den Marktsektor zu vergrößern. In den letzten Jahren hat die pharmazeutische Qualitätskontrollbranche der Medizin einige der bedeutendsten Vorteile geboten. Wichtige Akteure auf dem Markt für pharmazeutische Qualitätskontrolle, darunter BioMerieux SA SGS S.A., Charles River Laboratories International Inc., WiXi AppTec, Merck KGaA, Thermo Fisher Scientific Inc., Toxikon Corporation, Sartorius AG, REMI Group und Perkin Elmer, versuchen, die Marktnachfrage durch Investitionen in Forschung und Entwicklung von Products Tested zu steigern.
Die Entdeckung, Entwicklung, Herstellung und Lieferung von Proben und Geweben im Krankheitszustand für verarbeitete biologische Materialien, Forschung und Entwicklung, Immunoassay-Reagenzien sowie Produkte und Technologien zur Qualitätskontrolle werden alle von LGC Clinical Diagnostics Inc (LGC Clinical Diagnostics), ehemals SeraCare Life Sciences Inc., durchgeführt. Zu den Hauptangeboten des Unternehmens gehören digitale PCR-Instrumente, Kontrollen und Referenzmaterialien, SARS-COV-2, Plasma und Serumverdünnungsmittel und -derivate Sequenzierungstools der nächsten Generation und Zellkulturreagenzien. Um im Juni 2021 eine Vielzahl hochcharakterisierter genomischer Zelllinien-DNA und formalinfixierter, in Paraffin eingebetteter Standards mit nachweislich niedriger, mittlerer und hoher Mutationslast in ihren Exomregionen zu entwickeln, zu produzieren und bereitzustellen, hat SeraCare im Juni 2021 eine Partnerschaft mit dem International Quality Network for Pathology geschlossen.
Für den Einsatz in der Life-Science-Forschung, im Gesundheitswesen, in der analytischen Chemie und anderen Märkten entwickelt, produziert und vermarktet Bio-Rad Laboratories Inc (Bio-Rad) eine Vielzahl von Produkten und Systemen. Reagenzien, Geräte, Laborgeräte, Testsysteme, Informatiksysteme, Testkits und SpezifischeZu den Kernangeboten des Unternehmens gehören maßgeschneiderte Qualitätskontrollen. Um seinen Kunden ein komplettes Sortiment an InteliQ-Produkten und Unity QC-Datenmanagementsystemen sowie Kundenschulungen und Gerätewartung anzubieten, haben Bio-Rad und Roche Diagnostics im Mai 2021 eine Kooperation vereinbart.
Zu den wichtigsten Unternehmen auf dem Markt für pharmazeutische Qualitätskontrolle gehören
- BioMerieux SA SGS S.A.
- Charles River Laboratories International Inc.
- WiXi AppTec
- Merck KGaA
- Thermo Fisher Scientific Inc
- Toxikon Corporation
- Sartorius AG
- REMI-Gruppe
- Perkin Elmer
Entwicklungen in der pharmazeutischen Qualitätskontrollbranche
Mai 2019: emDie Erweiterung des Milbourn-Standorts des pharmazeutischen Dienstleistungslabors der Intertek Group Plc wurde angekündigt.
Marktsegmentierung für pharmazeutische Qualitätskontrolle
Produktausblick für die pharmazeutische Qualitätskontrolle
-
Verbrauchsmaterialien
-
Instrumente
-
Dienste
Analysetyp der pharmazeutischen Qualitätskontrolle
-
Sterilitätstests
-
Bioburden-Test
-
Endotoxintest
-
Stabilitätstest
-
Extrahierbar Auslaugbarkeitsprüfung
-
Rohstoffprüfung
-
Andere
Pharmazeutische Qualitätskontrollprodukte getestete Aussichten
-
Impfstoffe
-
Plasmaprodukt
-
Drogen
Regionaler Ausblick für die pharmazeutische Qualitätskontrolle
-
Nordamerika
-
USA
-
Kanada
-
Europa
-
Deutschland
-
Frankreich
-
Großbritannien
-
Italien
-
Spanien
-
Restliches Europa
-
Asien-Pazifik
-
China
-
Japan
-
Indien
-
Australien
-
Südkorea
-
Australien
-
Restlicher Asien-Pazifik-Raum
-
-
Rest der Welt
-
Naher Osten
-
Afrika
-
Lateinamerika
-
Bitte füllen Sie das folgende Formular aus, um ein kostenloses Muster dieses Berichts zu erhalten
Customer Stories

“This is really good guys. Excellent work on a tight deadline. I will continue to use you going forward and recommend you to others. Nice job”

“Thanks. It’s been a pleasure working with you, please use me as reference with any other Intel employees.”

“Thanks for sending the report it gives us a good global view of the Betaïne market.”

“Thank you, this will be very helpful for OQS.”

“We found the report very insightful! we found your research firm very helpful. I'm sending this email to secure our future business.”

“I am very pleased with how market segments have been defined in a relevant way for my purposes (such as "Portable Freezers & refrigerators" and "last-mile"). In general the report is well structured. Thanks very much for your efforts.”

“I have been reading the first document or the study, ,the Global HVAC and FP market report 2021 till 2026. Must say, good info! I have not gone in depth at all parts, but got a good indication of the data inside!”

“We got the report in time, we really thank you for your support in this process. I also thank to all of your team as they did a great job.”